
電話:
021-67610176傳真:
| 導讀 | 2018年5月25日,清華大學生命科學學院、結(jié)構(gòu)生物學高精尖創(chuàng)新中心施一公教授研究組就剪接體的組裝機理與結(jié)構(gòu)研究于《科學》(Science)雜志以長文形式再次發(fā)表重大研究成果。 |

本文轉(zhuǎn)載自“結(jié)構(gòu)生物學高精尖創(chuàng)新中心”,原標題:施一公研究組在《科學》發(fā)文報道處于激活前狀態(tài)的兩個*組裝的釀酒酵母剪接體高分辨率電鏡結(jié)構(gòu)。
這篇題為《*組裝的釀酒酵母剪接體激活前結(jié)構(gòu)》(Structures of the Fully Assembled Saccharomyces cerevisiae Spliceosome Before Activation)的論文報道了釀酒酵母剪接體處于被激活前階段的兩個*組裝的關(guān)鍵構(gòu)象——預(yù)催化剪接體前體(precursor pre-catalytic spliceosome,定義為“pre-B復合物”)和預(yù)催化剪接體(pre-catalytic spliceosome,定義為“B復合物”)。這兩個整體分辨率分別為3.3-4.6埃和3.9埃的高分辨率三維結(jié)構(gòu)展示了在剪接體組裝過程中pre-mRNA的5’剪接位點和分支點(BPS)的識別狀態(tài)與動態(tài)變化,回答了剪接體激活前pre-mRNA的5’剪接位點和分支點識別機理,以及激活過程中5’剪接位點和分支點如何逐步進入活性位點、剪接體如何逐步組裝并通過結(jié)構(gòu)重組zui終完成激活等重要問題。
RNA剪接是真核生物基因表達調(diào)控的重要環(huán)節(jié)之一。上世紀70年代,科學家們發(fā)現(xiàn)真核生物基因的不連續(xù)性,從而表明遺傳信息從DNA轉(zhuǎn)移到RNA上之后,需要經(jīng)歷有效遺傳信息的“剪斷”與重新“拼接”,這種有效遺傳信息的拼接與“無效”遺傳信息的去除,被稱為RNA剪接。RNA剪接普遍存在于真核生物中,隨著物種的進化,含有內(nèi)含子的基因數(shù)量增加,發(fā)生RNA剪接的頻率也相應(yīng)增高,使得一個基因編碼多個蛋白質(zhì)成為可能。RNA剪接的本質(zhì)是兩步轉(zhuǎn)酯反應(yīng),這種看似簡單的化學反應(yīng)在細胞中難以自行發(fā)生,而負責執(zhí)行這一化學反應(yīng)的是細胞核內(nèi)一個巨大且高度動態(tài)變化的分子機器——剪接體(spliceosome)。在剪接反應(yīng)過程中,多種蛋白質(zhì)-核酸復合物及剪接因子按照高度的順序發(fā)生結(jié)合和解聚,依次形成預(yù)組裝復合物U4/U6.U5 Tri-snRNP(U4/U6.U5三小核核糖核蛋白復合物)以及至少8個狀態(tài)的剪接體pre-B、B、Bact、B*、C、C*、P以及ILS復合物。
由于剪接體高度的動態(tài)性和復雜性,獲得不同狀態(tài)的剪接體的高分辨率三維結(jié)構(gòu)被*為世界難題。在這種巨大的挑戰(zhàn)下,施一公教授率領(lǐng)研究組迎難而上,經(jīng)過7年的努力,終于在2015年報道了裂殖酵母剪接體3.6埃的高分辨率結(jié)構(gòu),展示了剪接體催化中心近原子分辨率的結(jié)構(gòu)。這一重大研究成果對RNA剪接機理的研究產(chǎn)生革命性影響。自2015年*個剪接體結(jié)構(gòu)發(fā)表以后,施一公研究組相繼解析了釀酒酵母剪接體復合物處于6個不同狀態(tài)的高分辨率結(jié)構(gòu),分別是3.8埃的預(yù)組裝復合物U4/U6.U5 Tri-snRNP、3.5埃的激活狀態(tài)復合物Bact complex、3.4埃的*步催化反應(yīng)后復合物C complex、4.0埃的第二步催化激活狀態(tài)下的C* complex、3.6埃的完成兩步轉(zhuǎn)酯反應(yīng)后狀態(tài)下的P complex,以及3.5埃的內(nèi)含子套索剪接體ILS complex的結(jié)構(gòu)。這些已解析的剪接體基本覆蓋了整個RNA剪接循環(huán),從分子層面揭示了剪接體催化RNA剪接兩步反應(yīng)的工作機理,同時為理解剪接體的激活和解聚等過程的發(fā)生提供依據(jù)。然而,想要清楚解釋剪接體是如何逐步組裝并完成激活的機制仍有困難,而新發(fā)表的這篇文章所解析的兩個關(guān)鍵狀態(tài)的剪接體,則彌補了領(lǐng)域內(nèi)對這一部分研究的缺陷。
本文報道的處于激活前的兩個*組裝的剪接體結(jié)構(gòu),從復合物的提純、樣品的制備到結(jié)構(gòu)的解析,每一步都十分具有挑戰(zhàn)。預(yù)催化剪接體前體(pre-B complex)由U1 snRNP、U2 snRNP以及U4/U6.U5 tri-snRNP組成,目前被認為是組成蛋白zui多、分子量zui大的剪接體,該狀態(tài)結(jié)構(gòu)復雜,但各組分之間的相互作用并不緊密,使得該復合物在提純過程中十分容易解聚。在新發(fā)表的這篇《科學》文章中,施一公研究組對提純方案多次探索,zui終優(yōu)化出一套可以獲得穩(wěn)定的、性質(zhì)良好的pre-B complex樣品。隨后利用單顆粒冷凍電鏡技術(shù)重構(gòu)出了U1 snRNP、U2 snRNP以及U4/U6.U5 tri-snRNP部分分辨率高達3.3埃、3.6-4.6埃以及3.4埃的冷凍電鏡結(jié)構(gòu),并搭建了原子模型(圖1)。
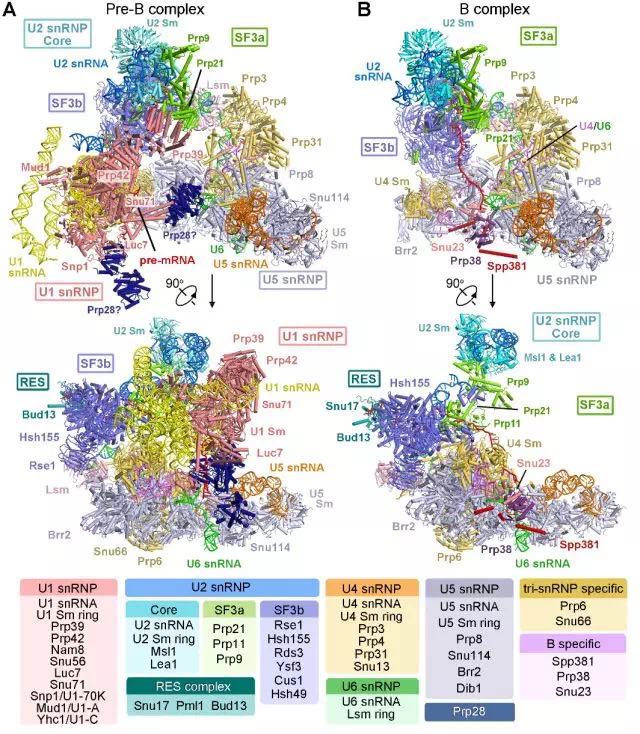
圖1 釀酒酵母預(yù)催化剪接體前體和
預(yù)催化剪接體的三維結(jié)構(gòu)
該文解析的pre-B complex結(jié)構(gòu)是目前世界上已解析的wei一一個同時包含五種核糖核蛋白(snRNP)剪接體結(jié)構(gòu),它由68個蛋白和6條RNA組成。在該結(jié)構(gòu)中,觀察到了剪接體組裝早期U1 snRNP對5’剪接位點的識別,以及五種核糖核蛋白之間的相互作用界面。與此同時,該文還報道了處于pre-B complex之后的另一個*組裝的剪接體,即預(yù)催化剪接體B complex的高分辨率三維結(jié)構(gòu)。結(jié)合B complex的結(jié)構(gòu)信息,通過結(jié)構(gòu)對比,可以清楚的看到在組裝過程中,pre-mRNA的5’剪接位點由一開始被U1 snRNP識別,而后由于構(gòu)象變化被轉(zhuǎn)移并與U6 snRNA配對,這一步的變化為剪接體激活提供了結(jié)構(gòu)基礎(chǔ)。除此之外,分支點的動態(tài)變化、剪接體的各組分所經(jīng)歷的結(jié)構(gòu)重組與構(gòu)象改變也都清晰的呈現(xiàn)出來。在文章zui后,根據(jù)pre-B的結(jié)構(gòu)特征,作者還大膽推測了zui早期的不*組裝的預(yù)剪接體(pre-spliceosome,定義為“A 復合物”)的三維結(jié)構(gòu)模型(圖2)。這兩個關(guān)鍵狀態(tài)剪接體結(jié)構(gòu)的解析,為揭示剪接體組裝初期如何識別5’剪接位點和分支點、如何進行結(jié)構(gòu)重組以及如何完成剪接體的激活等問題的機理提供了zui直接、有效的結(jié)構(gòu)證據(jù),也將為更高等真核生物可變剪接的研究提供結(jié)構(gòu)基礎(chǔ)與理論依據(jù)。
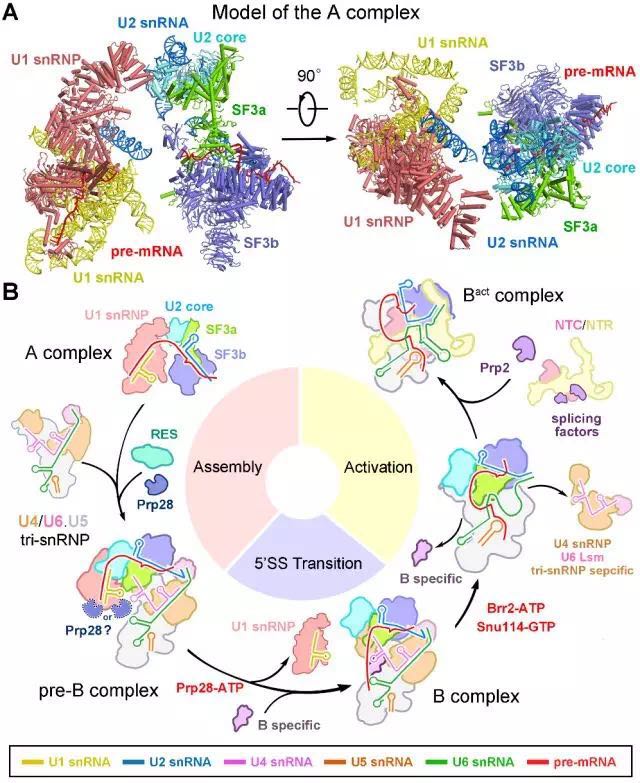
圖2 釀酒酵母預(yù)剪接體三維結(jié)構(gòu)的預(yù)測與
剪接體組裝并激活的模型
截至目前為止,施一公研究組在酵母中一共解析了9個不同狀態(tài)的剪接體高分辨的三維結(jié)構(gòu)(圖3),從組裝到被激活,從發(fā)生兩步轉(zhuǎn)酯反應(yīng)到剪接體的解聚,這9個狀態(tài)的剪接體完整覆蓋了剪接通路,將剪接體介導RNA剪接的過程串聯(lián)起來,為理解RNA剪接的分子機理提供了zui清晰、zui全面的結(jié)構(gòu)信息。
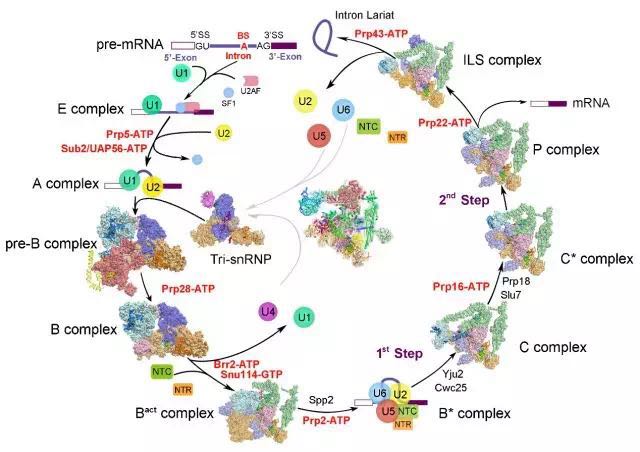
圖3 施一公研究組解析的酵母剪接體結(jié)構(gòu)匯總
(圖片來源: Shi Lab)
清華大學生命科學學院、結(jié)構(gòu)生物學高精尖創(chuàng)新中心施一公教授為本文的通訊作者;清華大學生命科學學院三年級博士研究生白蕊,醫(yī)學院博士后、結(jié)構(gòu)生物學高精尖創(chuàng)新中心學者萬蕊雪以及生命科學學院博士后、結(jié)構(gòu)生物學高精尖創(chuàng)新中心學者閆創(chuàng)業(yè)為該文的共同*作者;清華大學冷凍電鏡平臺的雷建林博士為冷凍電鏡數(shù)據(jù)收集提供了幫助。電鏡數(shù)據(jù)采集于清華大學冷凍電鏡平臺,計算工作得到清華大學高性能計算平臺、國家蛋白質(zhì)設(shè)施實驗技術(shù)中心(北京)的支持。本工作獲得了北京市結(jié)構(gòu)生物學高精尖創(chuàng)新中心及國家自然科學基金委的經(jīng)費支持。