
電話:
021-67610176傳真:
TAS-102,是一個日本研發的新型化療藥;本質上和卡培他濱(希羅達)、S-1(替吉奧)類似,都是口服的氟尿嘧啶類藥物。這個藥物,目前在國外已經被批準用于晚期腸癌的三線治療。近日,一項旨在探索TAS-102用于晚期胃癌的三線治療的三期臨床試驗,再次獲得成功,具體的數據,將會在近期的學術會議上宣布。
TAS-102用于晚期腸癌三線治療:死亡風險下降32%
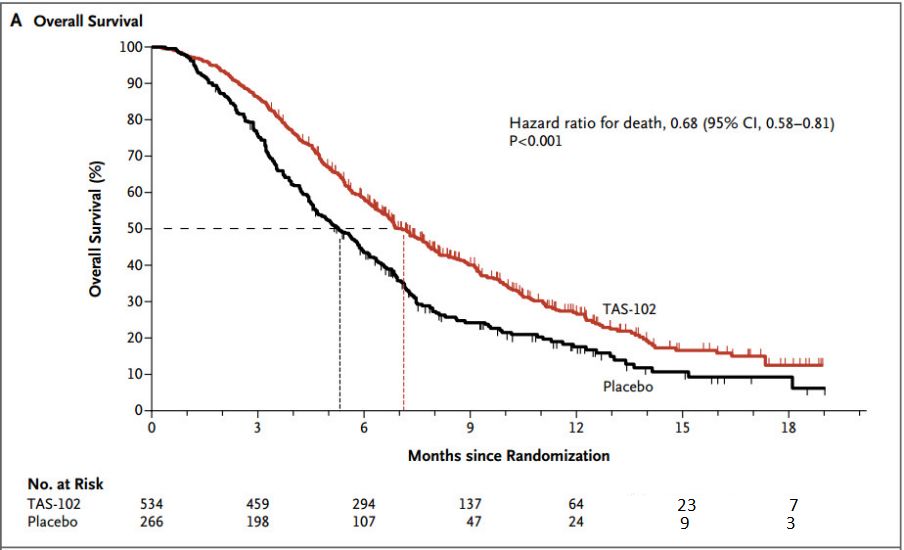
800名一線、二線標準治療失敗的難治性晚期腸癌患者,2:1分組,一組534名患者接受TAS-102治療,一組266名患者接受安慰劑治療。
結果顯示:TAS-102組的疾病控制率明顯更高(44% vs 16%)、生存期更長(7.1個月 vs 5.3個月),患者死亡風險下降32%。
副作用方面,TAS-102組的副作用主要是骨髓抑制(中性粒細胞減少發生率38%)、乏力、惡心、肝酶升高
TAS-102用于亞洲晚期腸癌患者:再獲成功
406名中國、韓國以及泰國難治性晚期腸癌患者,按照2:1的比例,一組接受TAS-102治療,一組接受安慰劑治療。結果提示:TAS-102組生存期明顯更長(7.8個月 vs 7.1個月)。而嚴重不良反應發生率,在TAS-102和安慰劑組,基本相當(亞洲人對TAS-102這個口服藥,耐受性不錯)。
TAS-102用于晚期胃癌三線治療:三期臨床試驗大獲成功
日前,探索TAS-102用于胃癌三線治療的三期臨床試驗TAGS,宣布獲得成功,具體數據尚未公布
不過,TAS-102用于難治性胃癌挽救治療的二期臨床試驗數據,已經公布。29名患者入組,接受TAS-102治療,35mg/m2 每天2次。疾病控制率65.5%,中位無疾病進展生存時間為2.9個月,中位總生存時間為8.7個月。
zui常見的3-4級不良反應主要是:中性粒細胞減少、白細胞減少、貧血以及食欲下降。