
電話:
021-67610176傳真:
近日,一項刊登在雜志Advanced Materials上的研究報告中,來自賓夕法尼亞大學的生物工程學家通過研究利用諸如轉移性癌細胞等疾病細胞的*機械特性,就能幫助改善藥物療法運輸,從而更好地靶向作用疾病細胞來治療相關疾病。
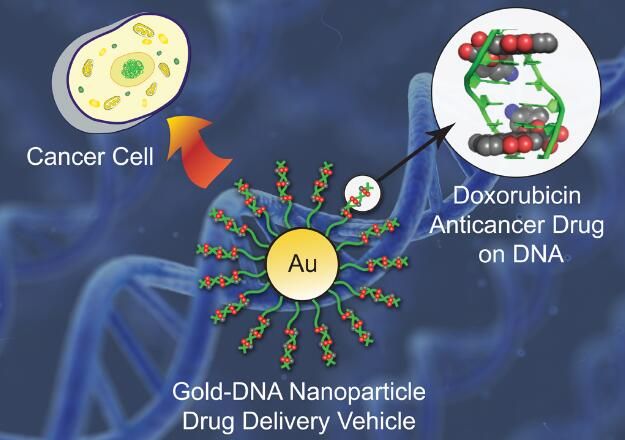
目前很多實驗室都在開發基于納米顆粒的藥物運輸系統來選擇性靶向作用腫瘤組織,而這依賴于一種鎖鑰系統,即納米顆粒表面的蛋白“鑰匙”能夠進入到癌細胞表面高水平表達蛋白的“鎖”中,隨后細胞膜就會將納米顆粒包裹起來并且吸收掉,如果足夠的納米顆粒和其藥物“貨物”被攝入的話,癌細胞就會死亡。
研究者Sulin Zhang表示,鎖鑰之間的粘合力是驅動納米顆粒進入癌細胞的關鍵;而無論何時,只要產生一個驅動力,就會出現相應的阻力;這種驅動力具有一定的生物化學特性,即蛋白-蛋白之間的相互作用。這種阻力就是細胞膜包裹納米顆粒所需要的機械能成本,截止到目前為止,生物工程學家們僅考慮到了驅動力,并且設計出了能優化化學反應的納米顆粒,這種靶向策略稱之為“化療靶向作用”(chemotargeting),研究人員認為,他們還應該考慮細胞的機械特性,并且設計出納米顆粒能夠增強這種靶向作用,于是這就形成了一種新型的靶向系統,即“機械靶向作用”(mechanotargeting)。
這兩種靶向系統是互補的,你可以將兩種系統結合起來,實現基于納米顆粒的診療目的,實際上,靶向作用的效率需要驅動力和阻力之間的巧妙平衡過程,比如,如果納米顆粒表面有過多的“鑰匙”的話,盡管這些鑰匙技能與正常細胞上不匹配的“鎖”發生微弱的相互作用,這些微弱的脫靶效應也會為納米顆粒提供足夠的粘合能量來促進其滲透入細胞膜,并且殺滅健康細胞。
從另一方面來講,如果粘合能量不夠高的話,納米顆粒就不會進入到細胞內部。這項研究中,研究人員發表了對生長在可變硬度的水凝膠上癌細胞的實驗結果。當位于較軟的水凝膠上時,細胞就會保持粘性,并會經歷幾乎恒定的壓力,從而就能限制對納米顆粒的吸收,但當位于較硬的水凝膠上時,細胞就會具有轉移性,并且會形成三維形狀,為納米顆粒提供更多的表面區域進入,而且會變得壓力特性較小;在這種情況下,細胞攝入納米顆粒的數量就是良性細胞的5倍。
后研究者Zhang說道,這種納米顆粒具有一定的熒光特性,因此我們就能通過熒光強度的大小來計算進入到細胞中的納米顆粒的水平,而且我們還發現,惡性細胞的熒光強度要高于良性細胞5倍,這就證實了我們所開發的“機械靶向系統”能正常發揮作用。(生物谷)
原始出處:
Qiong Wei, Changjin Huang, Yao Zhang, et al. Mechanotargeting: Mechanics-Dependent Cellular Uptake of Nanoparticles. Advanced Materials, 2018; 1707464 DOI: 10.1002/adma.201707464