開發出對線粒體DNA進行基因編輯的MitoTALEN和mtZFN
發布日期:2018-09-26 瀏覽次數:1609
在兩項新的研究中,來自美國和和歐洲的研究人員使用兩種基因編輯方法來校正活小鼠中的線粒體突變。相關研究結果于2018年9月24日在線發表在Nature Medicine期刊上,論文標題分別為“MitoTALEN reduces mutant mtDNA load and restores tRNAAla levels in a mouse model of heteroplasmic mtDNA mutation”和“Genome editing in mitochondria corrects a pathogenic mtDNA mutation in vivo”。這些研究結果表明兩種基因編輯工具---轉錄激活子樣效應因子核酸酶(TALEN)和鋅指核酸酶(ZFN)---可能有朝一日能夠治療人類所患的某些線粒體疾病。
線粒體DNA(mtDNA)中發生的致病性突變會導致從肌肉無力到心臟病的癥狀,而且在每5000名成年人中,大約就有1人會發生這樣的致病性突變。雖然三親體外受精(three-parent IVF)---一種有爭議的方法,它除了使用母親的卵核和父親的精子之外,還使用了第三人的線粒體---已被提出作為一種避免mtDNA突變遺傳的方法,但是當前還沒有治療出生時就攜帶著這種缺陷的人的方法。美國梅約診所分子遺傳學家Stephen Ekker (未參與這兩項研究)表示,“這在很大程度上是一種未得到滿足的需求。”
CRISPR基因編輯技術在對細胞核DNA中發現的突變進行編輯方面取得了快速進展,但是科學家們很難將這種相同的技術應用于線粒體DNA,這是因為線粒體似乎不會攝取讓CRISPR系統靶向合適序列的向導RNA(gRNA)。在這兩項新的研究中,研究人員使用了較老的不需要gRNA的基因編輯方法。
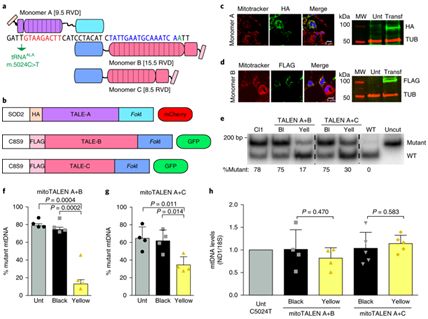
圖片來自Nature Medicine, doi:10.1038/s41591-018-0166-8。
在項研究中,來自美國邁阿密大學的Carlos Moraes及其同事們將含有靶向線粒體的TALEN(mitochondrial-targeted TALEN, MitoTALEN)的腺相關病毒(AAV)注射到攜帶著mtDNA突變的小鼠肌肉中。在六個月后,小鼠肌肉組織中的突變mtDNA的水平下降了50%以上---低于通常與線粒體疾病的癥狀相關的水平。
在第二項研究中,在由英國劍橋大學的一個研究小組領導下,研究人員將含有靶向線粒體的ZFN(mitochondrially targeted zinc-finger nuclease, mtZFN)的AAV病毒注射到小鼠的尾靜脈中,從而被系統性地運送到心臟中。僅兩個多月后,突變mtDNA的水平在心臟組織中下降了大約40%。
美國哥倫比亞大學歐文醫學中心線粒體生物學家Martin Picard(未參與這兩項研究)表示,“這些都是非常出色的發現,使得人們可能考慮在人類身上做到這一點。”據報道,這兩個研究團隊均計劃開展臨床試驗。(生物谷 )
參考資料:
Sandra R. Bacman, Johanna H. K. Kauppila, Claudia V. Pereira et al.MitoTALEN reduces mutant mtDNA load and restores tRNAAla levels in a mouse model of heteroplasmic mtDNA mutation. Nature Medicine, Published Online: 24 September 2018, doi:10.1038/s41591-018-0166-8.
Payam A. Gammage, Carlo Viscomi, Marie-Lune Simard et al. Genome editing in mitochondria corrects a pathogenic mtDNA mutation in vivo. Nature Medicine, Published Online: 24 September 2018, doi:10.1038/s41591-018-0165-9.

